がん研究の「見えない世界」が明らかに
がんの診断法が、根本から書き換えられようとしている。
私たちは何十年もの間、がんを「異常なヒト細胞の塊」として見てきた。医師たちは変異遺伝子、放射線、化学療法に焦点を当て、腫瘍をいかに縮小・除去するかに心血を注いできた。
しかし、すべての腫瘍には、私たちが真に見てこなかった「もう一つの世界」が隠されていた。それは、腫瘍自身が持つ微生物生態系――細菌、真菌、ウイルスが織りなす複雑なコミュニティである。
最新の世界規模研究により、この「見えない世界」がついに解明された。そしてこの発見は、がんの検出方法と治療法を根底から変える可能性を秘めている。
重要ポイント:
- すべての腫瘍に独自の微生物生態系が存在
- がんの種類ごとに異なる「微生物の指紋」がある
- 血液検査で微生物の痕跡を読み取り、早期発見が可能に
- 10年以内の臨床応用を研究者が予測
- 治療反応の予測と個別化医療の実現へ
従来のがん研究が見逃してきた「盲点」
従来のがん研究は、腫瘍を孤立した侵略者のように扱ってきた。
がん細胞の増殖メカニズム、遺伝子変異のパターン、免疫系との相互作用――これらはすべて「ヒト細胞」だけに焦点を当てた研究だった。医師たちは腫瘍の大きさ、形状、転移の有無を測定し、どの薬剤が効くかを試行錯誤してきた。
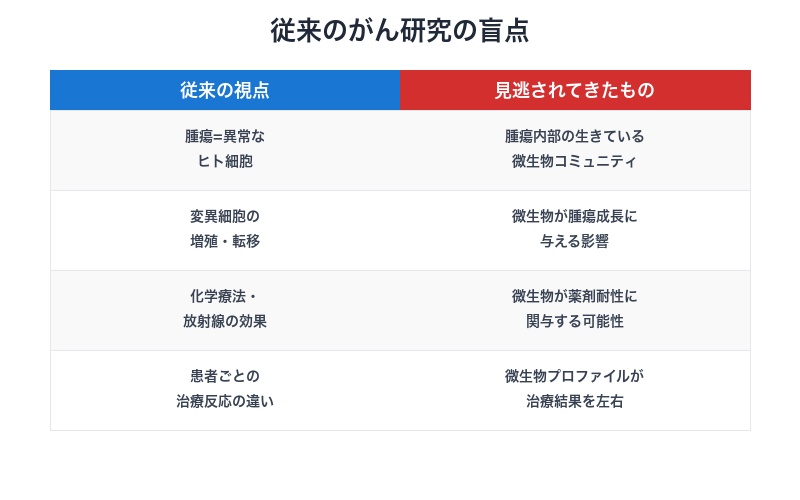
しかし、この視点には決定的な盲点があった。
| 従来の視点 | 見逃されてきたもの |
|---|---|
| 腫瘍=異常なヒト細胞の塊 | 腫瘍内部の生きている微生物コミュニティ |
| 変異細胞の増殖・転移 | 微生物が腫瘍の成長・治療反応に与える影響 |
| 化学療法・放射線の効果 | 微生物が薬剤耐性に関与する可能性 |
| 患者ごとの治療反応の違い | 腫瘍の微生物プロファイルが治療結果を左右 |
なぜ一部の患者は治療に劇的に反応し、他の患者はまったく反応しないのか――この謎に対し、医師たちは「個人差」や「腫瘍の特性」という曖昧な答えで推測するしかなかった。
しかし真の答えは、腫瘍内部の「見えない住人たち」にあったのかもしれない。
腫瘍内微生物生態系の発見:各がんに固有の「バーコード」
学術誌『Genes & Diseases』に発表された画期的な研究により、ヒト腫瘍内部の「微生物の指紋」が解明された。
この発見は衝撃的だ。すべての腫瘍は、細菌・真菌・ウイルスの特有な混合物を保持している。そしてこの微生物の組み合わせは、がんの種類によって明確に異なるのだ。
腫瘍内で発見された微生物の種類
研究者たちが腫瘍内部から特定した主要な微生物グループ:
- 細菌:Proteobacteria(プロテオバクテリア)、Firmicutes(ファーミキューテス)、Streptococcus(連鎖球菌)、Neisseria(ナイセリア)、Actinobacteria(放線菌)、Fusobacterium nucleatum(フソバクテリウム・ヌクレアタム)
- ウイルス:HPV(ヒトパピローマウイルス)、CMV(サイトメガロウイルス)
- その他の微生物:Chlamydia(クラミジア)、Mycoplasma(マイコプラズマ)、各種真菌
これらの微生物は、腫瘍内部で複雑なコミュニティを形成し、まるでバーコードのように各がんに固有の生物学的特徴を刻み込んでいる。

がんの種類別「微生物の指紋」:診断の新基準
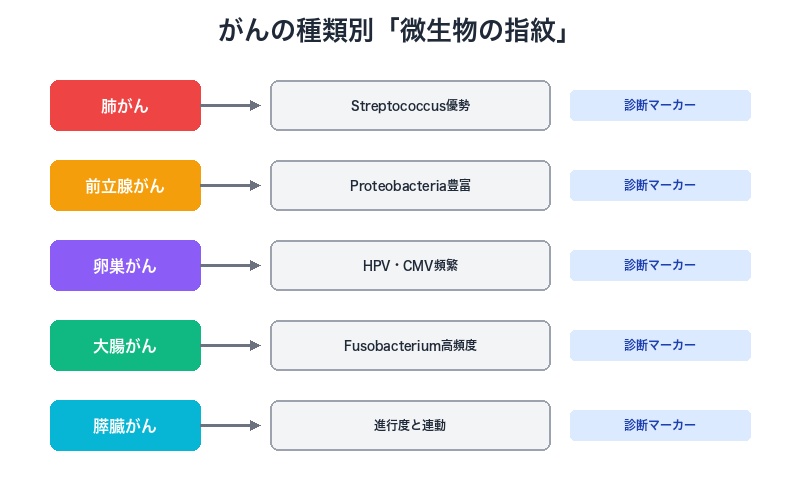
最も驚くべき発見は、がんの種類ごとに微生物の組成が劇的に異なるという事実だ。
| がんの種類 | 微生物の特徴 | 臨床的意義 |
|---|---|---|
| 肺がん | 細菌多様性が低い Streptococcus・Neisseriaが優勢 |
微生物プロファイルで肺がんのサブタイプ識別 |
| 前立腺がん | Proteobacteria・Actinobacteriaが豊富 | 微生物多様性が予後と関連 |
| 卵巣がん | Firmicutes・Proteobacteria HPV・CMV感染が頻繁 |
ウイルス検出で早期診断の可能性 |
| 大腸がん | Fusobacterium nucleatumが高頻度 | 微生物組成が腫瘍ステージ・生存率と相関 |
| 膵臓がん | 微生物組成が腫瘍進行度と連動 | 治療反応の予測マーカーとして活用 |
この「微生物の指紋」は、各がんを識別するための新しいバイオマーカーとなる可能性がある。従来のがんマーカー(CEA、CA19-9など)よりも精密で、早期段階での検出が期待できるのだ。
診断革命:血液検査で「微生物の痕跡」を読み取る
この発見が真に革命的なのは、診断方法を根本から変える可能性があるからだ。
従来のがん検診は、画像診断(CT・MRI)や生検(組織採取)に依存してきた。これらの方法は侵襲的で、がんが一定の大きさに成長するまで検出できない。
しかし、腫瘍の微生物バーコードを利用すれば、まったく新しいアプローチが可能になる。
微生物バーコード診断の可能性
未来の診断シナリオ:
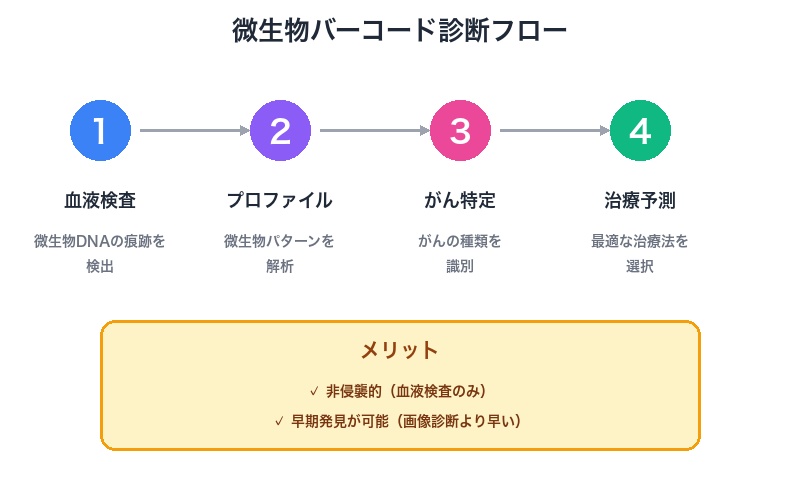
- 血液検査で微生物DNAの痕跡を検出
腫瘍から血液中に放出される微生物の遺伝子断片を、次世代シーケンサーで解析 - 微生物プロファイルからがんの種類を特定
「肺がんパターン」「大腸がんパターン」など、微生物の指紋でがんのタイプを識別 - 腫瘍の内部生態系から治療反応を予測
微生物の組成を知るだけで、どの治療法が効くかを事前に判断 - リキッドバイオプシーとの統合
循環腫瘍DNA(ctDNA)検査と微生物バーコード検査を組み合わせ、精度を向上
想像してほしい。定期的な血液検査で、がんを画像診断よりも早く、非侵襲的に検出できる未来を。これは「精密医療が真に精密になる」瞬間だ。
治療への影響:腫瘍の「生息環境」を標的にする
微生物バーコードの発見は、診断だけでなく治療戦略も変える。
従来の治療法は「がん細胞を殺す」ことに集中してきた。しかし、腫瘍内の微生物が薬剤耐性や治療反応に影響を与えているとしたら、治療のアプローチ自体を見直す必要がある。
腫瘍マイクロバイオームを標的にした新治療法
| 治療戦略 | アプローチ | 期待される効果 |
|---|---|---|
| 微生物プロファイル ベースの治療選択 |
腫瘍の微生物組成を解析し、最適な化学療法を選択 | 治療反応率の向上 無駄な治療の回避 |
| 抗生物質併用療法 | 特定の細菌を標的にした抗生物質を化学療法と併用 | 薬剤耐性の克服 治療効果の増強 |
| プロバイオティクス 介入 |
有益な微生物を導入し、腫瘍環境を改変 | 免疫反応の活性化 腫瘍増殖の抑制 |
| ファージ療法 | 特定の腫瘍内細菌を標的にしたバクテリオファージ投与 | 腫瘍微生物の選択的除去 副作用の最小化 |
研究者らは、「がんそのものだけでなく、その生息環境全体を治療する」という新しいパラダイムを提唱している。これは、がん治療における根本的な発想の転換だ。

10年以内の臨床応用へ:実現に向けた課題
研究者たちは、この技術が10年以内に臨床現場で使用可能になると見ている。
しかし、実現には複数の課題をクリアする必要がある。
臨床応用に向けた課題と展望
- 因果関係の解明
微生物が腫瘍の原因なのか、それとも腫瘍環境に適応した結果なのか――現在の研究では相関関係が示されているが、因果関係の証明が必要 - 大規模臨床試験
数千人規模の患者データを収集し、微生物バーコードの診断精度・予測精度を検証 - 標準化された検査プロトコル
微生物DNAの抽出・シーケンス・解析方法を標準化し、再現性を確保 - 規制当局の承認
FDA(米国食品医薬品局)やEMA(欧州医薬品庁)の承認プロセスを経る必要がある - コストの削減
次世代シーケンシングのコストを下げ、保険適用可能な価格帯に
現在、複数の研究機関とバイオテクノロジー企業が、この分野への投資を加速させている。「微生物バーコード検査キット」の商品化も、近い将来に実現する可能性がある。

がん治療の新時代:「見えない世界」とのバランス
この研究が私たちに示す新たな真実は、シンプルだが深い。
「がんを治すとは、私たちの体内に存在する見えない世界のバランスを取り戻すことかもしれない」
私たちの体は、単独で存在しているわけではない。腸内細菌叢、皮膚マイクロバイオーム、そして腫瘍内の微生物コミュニティ――これらすべてが、私たちの健康と病気に深く関わっている。
がん研究は、ついに「ヒト細胞だけを見る」段階から、「微生物との共生を理解する」段階へと進化しようとしている。
今後の展望:
- 年1回の血液検査で、がんを早期発見できる時代
- 微生物プロファイルに基づく、完全な個別化医療
- 化学療法の効果を事前に予測し、無駄な治療を回避
- 抗生物質やプロバイオティクスを併用した、副作用の少ない治療法
- 腫瘍の「生態系全体」を標的にした、新世代のがん治療薬
がん研究は今、歴史的な転換点に立っている。毎週のように新たなブレイクスルーが報告され、私たちは「がん治癒」という人類の夢に、着実に近づいている。
腫瘍内の「微生物の指紋」という発見は、その夢の実現を大きく加速させるだろう。次の10年で、がん診断と治療は、私たちの想像を超えて進化するはずだ。
Every week there are new breakthroughs in cancer research, bringing us closer and closer to a cure!
— Chubby♨️ (@kimmonismus) November 1, 2025
https://t.co/vlE82c4ZXQ


コメント