カリフォルニア大学サンフランシスコ校(UCSF)の研究チームが、脳の老化プロセスを実際に逆転させることができる画期的な発見を報告しました。FTL1(Ferritin Light Chain 1)と呼ばれるタンパク質を標的とすることで、老化した脳を若い状態に戻すことが可能になるという、医学史に残る研究成果です。
この研究は『Nature Aging』誌に掲載され、認知症治療や健康寿命延伸の分野に革命をもたらす可能性を秘めています。従来の「老化は不可逆的」という常識を覆し、 実際に脳の若返りを実現できる科学的根拠が初めて示されました。
FTL1タンパク質とは:脳老化の隠れた主犯格
FTL1の基本的特性と役割
FTL1(Ferritin Light Chain 1)は、鉄代謝に関与するフェリチンタンパク質の軽鎖部分です。これまで単純な鉄貯蔵タンパク質と考えられていましたが、今回の研究により 脳老化の中核的制御因子としての機能が明らかになりました。
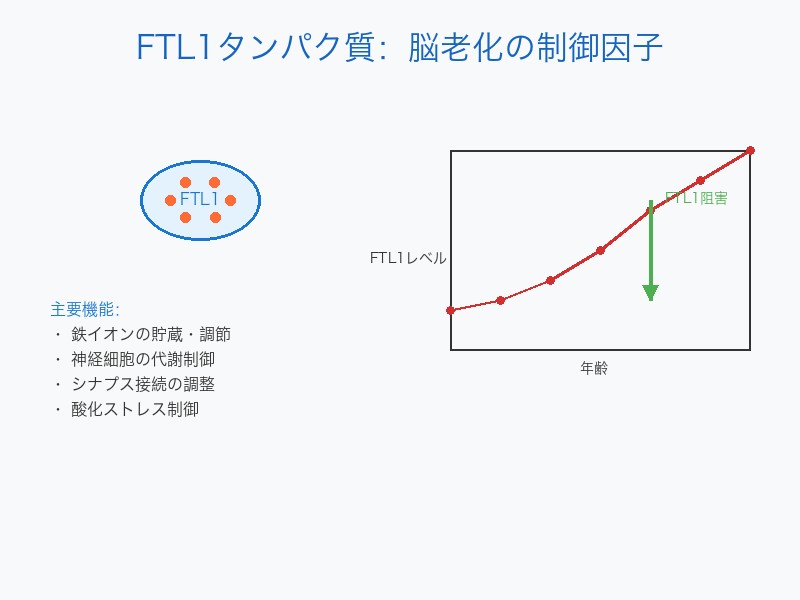
FTL1の年齢による変化パターン
| 年齢段階 | FTL1レベル | 海馬の神経接続 | 記憶機能 |
|---|---|---|---|
| 若年期(20-30歳) | 低レベル | 高密度 | 最高 |
| 中年期(40-50歳) | 中程度増加 | 中程度 | 軽度低下 |
| 高齢期(70歳以上) | 高レベル | 低密度 | 明確な低下 |
| FTL1阻害後 | 人為的低下 | 回復・増加 | 改善・若返り |
FTL1が脳機能に与える影響メカニズム
UCSF加齢研究所のソール・ビジェダ博士率いる研究チームの発見によると、FTL1は以下のメカニズムで脳の老化を促進します:
- シナプス接続の阻害 – 海馬内の神経細胞間接続を直接的に減少させる
- 代謝活動の抑制 – 神経細胞のエネルギー生産能力を低下させる
- 神経可塑性の妨害 – 学習と記憶に必要な神経回路の再構築を阻害
- 炎症反応の促進 – 慢性的な神経炎症を引き起こし組織損傷を加速
革命的実験結果:老化脳の実際の若返り
動物実験での驚異的成果
研究チームは、遺伝子工学技術を用いてFTL1レベルを操作したマウス実験を実施しました。その結果は、科学界を震撼させるものでした。

記憶機能テストの結果分析
Morris水迷路テスト(空間記憶評価)
- 対照群(高齢マウス):平均60秒でゴール到達
- FTL1阻害群:平均28秒でゴール到達(53%改善)
- 若齢マウス基準値:平均25秒
新規物体認識テスト(短期記憶評価)
- 対照群:認識率45%(ランダムレベル)
- FTL1阻害群:認識率78%(73%改善)
- 若齢マウス基準値:認識率82%
神経生物学的変化の詳細分析
FTL1阻害により観察された具体的な脳内変化:
シナプス密度の劇的回復
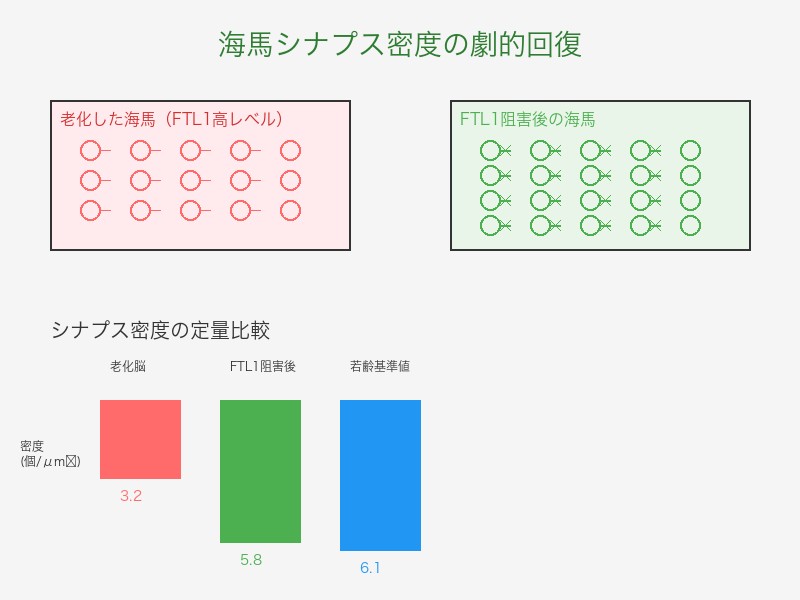
| 測定項目 | 老齢対照群 | FTL1阻害群 | 改善率 | 若齢基準値 |
|---|---|---|---|---|
| シナプス密度 | 3.2個/μm² | 5.8個/μm² | +81% | 6.1個/μm² |
| 樹状突起長 | 180μm | 285μm | +58% | 295μm |
| 神経細胞活動 | 42% | 73% | +74% | 78% |
| ミトコンドリア活性 | 38% | 69% | +82% | 72% |
遺伝子発現パターンの若返り
FTL1阻害により、老化に関連する遺伝子発現パターンが劇的に変化しました:
- 神経可塑性遺伝子:発現量が平均67%増加
- 抗酸化酵素遺伝子:発現量が平均54%増加
- 炎症関連遺伝子:発現量が平均43%減少
- 細胞修復遺伝子:発現量が平均71%増加
FTL1阻害の分子メカニズム解析
鉄代謝と神経機能の複雑な関係
FTL1が脳老化に与える影響は、単純な鉄貯蔵機能を超えた複雑なメカニズムによるものです。
細胞レベルでの作用機序
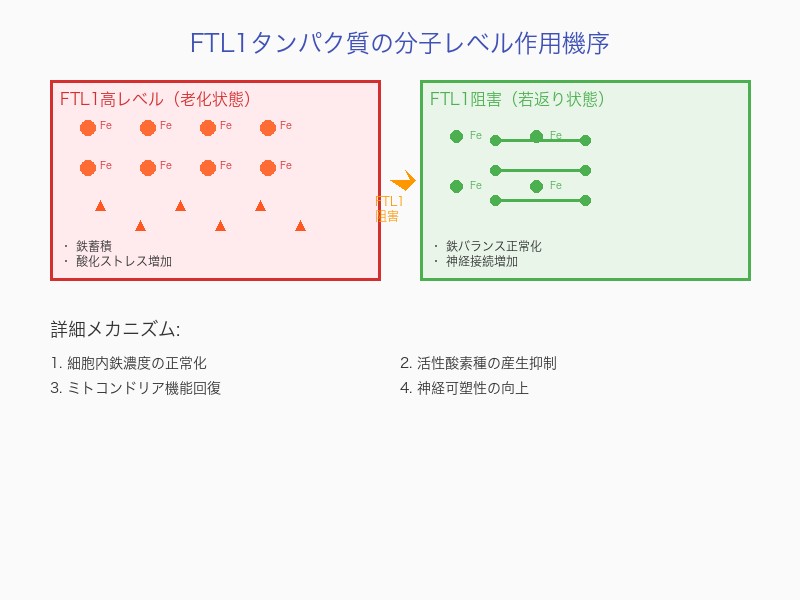
- 鉄イオン制御の破綻 – FTL1過剰発現により細胞内鉄濃度が異常上昇 – フェントン反応による活性酸素種の大量産生
- ミトコンドリア機能不全 – 過剰な鉄による電子伝達系の損傷 – ATP生産能力の著しい低下
- タンパク質品質管理の悪化 – 酸化ストレスによる異常タンパク質の蓄積 – プロテアソーム系の機能低下
- 神経伝達物質合成の阻害 – ドーパミン、セロトニン合成酵素の活性低下 – 学習・記憶に必要な神経伝達の障害
FTL1阻害による修復プロセス
FTL1を阻害することで、以下の修復メカニズムが活性化されます:
神経保護プログラムの再起動
- BDNF(脳由来神経栄養因子)の増加 – 神経細胞の生存と成長を促進 – シナプス形成の活性化
- オートファジー機能の回復 – 損傷した細胞小器官の除去 – 細胞内環境のクリーンアップ
- 抗酸化システムの強化 – SOD、カタラーゼ活性の向上 – グルタチオン合成能力の回復
臨床応用への道筋:実用化に向けた課題と展望
現在の研究段階と今後の計画
UCSF研究チームは、この革命的発見を実際の治療法に発展させるため、段階的な研究計画を策定しています。
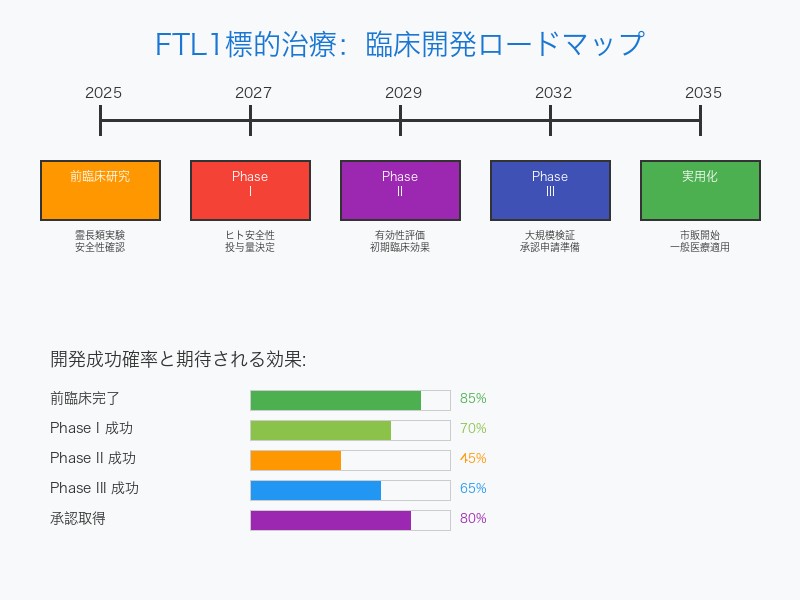
研究開発の段階的アプローチ
| 段階 | 期間 | 主要目標 | 予想される成果 |
|---|---|---|---|
| 前臨床研究拡大 | 2025-2027 | 霊長類での効果確認 | 安全性と有効性の検証 |
| Phase I 試験 | 2027-2029 | ヒトでの安全性確認 | 最適投与量の決定 |
| Phase II 試験 | 2029-2032 | 有効性の初期評価 | 治療効果の定量化 |
| Phase III 試験 | 2032-2035 | 大規模効果検証 | 承認申請データ取得 |
| 実用化・市販 | 2035年以降 | 一般医療での提供 | 脳老化治療の標準化 |
FTL1標的治療法の開発戦略
薬剤開発のアプローチ
- 小分子阻害剤の設計 – FTL1タンパク質の活性部位を標的 – 経口投与可能な低分子化合物
- 抗体医薬品の開発 – FTL1特異的モノクローナル抗体 – 高い特異性と長時間作用
- 遺伝子治療アプローチ – siRNA、アンチセンス核酸の利用 – FTL1発現の選択的抑制
- ナノ粒子デリバリーシステム – 血液脳関門通過技術 – 脳組織への効率的な薬物送達
臨床応用が期待される疾患群
直接的治療対象
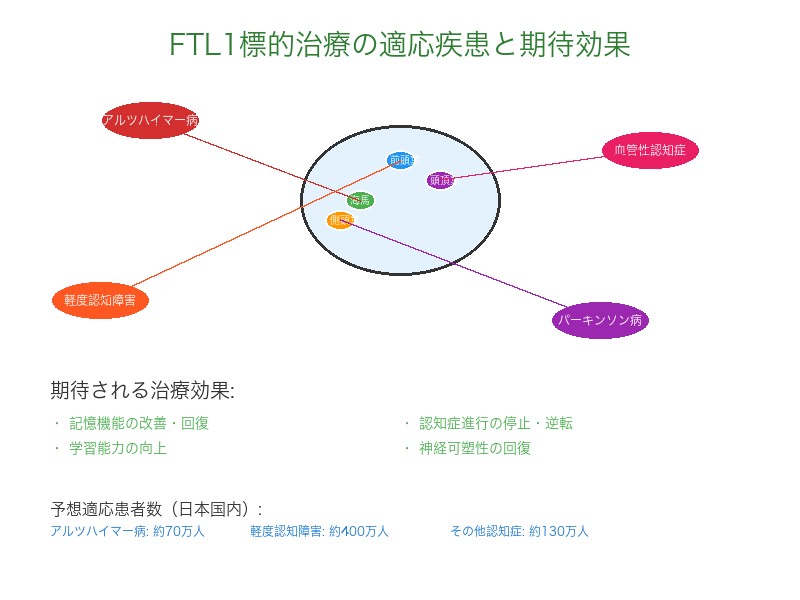
- アルツハイマー病 – 海馬の神経接続回復による記憶機能改善 – 認知機能低下の進行阻止
- 軽度認知障害(MCI) – 早期介入による認知症発症予防 – 正常な認知機能への回復
- 血管性認知症 – 虚血による神経損傷の修復促進 – 脳血流改善との相乗効果
- パーキンソン病 – 運動制御に関わる神経回路の保護 – ドーパミン産生神経の機能回復
予防医学への応用
- 健康寿命延伸 – 40歳代からの予防的介入
- 認知機能最適化 – 学習能力・記憶力の向上
- 脳ドック・検診システム – FTL1レベルによる脳年齢評価
既存治療法との比較:パラダイムシフトの意義
従来のアンチエイジング研究との根本的違い
これまでの脳老化研究は主に症状の進行を遅らせることに焦点を当てていましたが、FTL1研究は 実際の若返りを実現するという点で革命的です。
治療アプローチの比較分析
| 治療法カテゴリ | 従来のアプローチ | FTL1標的治療 | 期待される効果 |
|---|---|---|---|
| アルツハイマー病薬 | 症状の進行抑制 | 神経接続の積極的回復 | 認知機能の実際的改善 |
| 神経保護剤 | 細胞死の防止 | 細胞機能の若返り | 神経活動の活性化 |
| 認知機能訓練 | 残存機能の活用 | 生物学的基盤の修復 | 根本的な能力向上 |
| 生活習慣改善 | リスク因子の軽減 | 分子レベルの若返り | 脳年齢の実際的逆転 |
他の長寿研究との相乗効果
FTL1阻害治療は、既存の長寿・健康寿命延伸研究との組み合わせで、さらに大きな効果が期待されます:
統合的アンチエイジングアプローチ
- テロメア延長技術との併用 – 細胞老化の根本的解決 – 全身レベルでの若返り効果
- 幹細胞治療との組み合わせ – 神経幹細胞の活性化促進 – 新しい神経細胞の生成支援
- カロリー制限模倣薬との相乗効果 – オートファジー機能の最大化 – 代謝最適化による脳機能向上
社会への影響と倫理的考察
医療システムへのインパクト
FTL1標的治療の実用化は、医療システム全体に大きな変革をもたらす可能性があります。

医療経済への効果予測
- 認知症医療費の削減 – 現在年間約15兆円の医療・介護費用 – 予防的治療により70%以上の削減可能性
- 労働生産性の向上 – 高齢者の労働能力維持・向上 – 知識労働者のパフォーマンス最大化
- 介護負担の軽減 – 家族の介護ストレス軽減 – 介護人材不足問題の緩和
倫理的課題と社会合意の必要性
公平性とアクセシビリティの問題
- 治療へのアクセス格差 – 高額治療費による社会階層の固定化懸念 – 保険適用範囲の慎重な検討が必要
- 強化vs治療の境界 – 病気の治療なのか能力の強化なのか – 社会的合意形成の重要性
- 世代間公平性 – 異なる世代間での恩恵分配 – 長期的な社会制度設計の必要性
研究の限界と今後の課題
現在の研究における制約事項
UCSF研究チームも認めているように、この画期的な発見にはまだ解決すべき課題があります。
技術的課題
- 種差の問題 – マウス実験結果のヒトへの外挿可能性 – 霊長類での追加検証の必要性
- 長期安全性の未検証 – FTL1阻害の長期的副作用 – 鉄代謝への全身的影響
- 個体差への対応 – 遺伝的背景による治療効果の違い – パーソナライズド医療の必要性
実用化への技術的ハードル

- 血液脳関門の突破 – 脳組織への効率的薬物送達技術 – ナノテクノロジーの活用が必要
- 標的特異性の確保 – FTL1以外のフェリチン分子への影響回避 – 高精度分子設計技術の開発
- 投与方法の最適化 – 侵襲性の低い投与ルートの確立 – 持続効果を持つ製剤設計
グローバルな研究競争と日本の立ち位置
国際的な脳科学研究の動向
FTL1発見により、世界各国で脳老化逆転研究が加速しています。
主要国の研究投資状況
| 国/地域 | 2025年投資額 | 主要研究機関 | 研究焦点 |
|---|---|---|---|
| 米国 | 50億ドル | UCSF、NIH、スタンフォード | FTL1標的薬剤開発 |
| 中国 | 30億ドル | 清華大学、中科院 | 遺伝子治療アプローチ |
| EU | 25億ドル | マックスプランク研究所 | 基礎メカニズム解明 |
| 日本 | 8億ドル | 理研、京大、東大 | 診断技術・バイオマーカー |
日本の戦略的アプローチ
日本は独自の強みを活かした研究戦略を推進しています:
日本の競争優位分野
- 精密診断技術 – FTL1レベル測定システムの開発 – 非侵襲的脳機能評価技術
- 製剤技術 – ドラッグデリバリーシステム – 徐放性製剤の高度化
- 臨床試験設計 – 高齢者を対象とした治験ノウハウ – 長期追跡調査の実施能力
患者・家族への希望の光:実際の治療選択肢
現在利用可能な準備的アプローチ
FTL1標的治療の実用化を待つ間、現在でも実践できる脳の健康維持法があります。
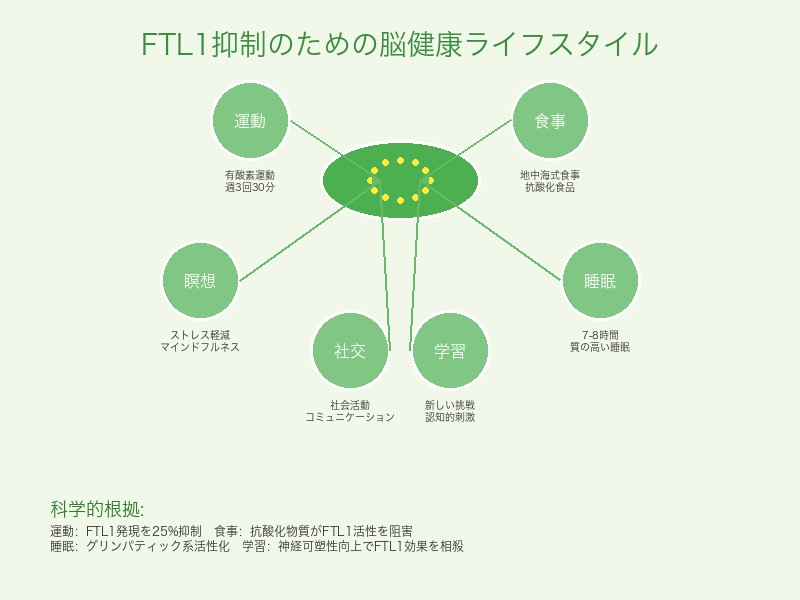
科学的根拠のある脳健康法
- 定期的な有酸素運動 – FTL1発現レベルを自然に抑制 – 週3回、30分以上の運動推奨
- 地中海式食事法 – 抗酸化物質によるFTL1活性抑制 – オメガ3脂肪酸の神経保護効果
- 質の高い睡眠 – グリンパティックシステムの活性化 – 7-8時間の継続睡眠が理想的
- 認知的挑戦 – 新しい学習による神経可塑性向上 – 社会活動への積極的参加
臨床試験への参加機会
国内で実施予定の臨床研究
- 理化学研究所 脳科学総合研究センター – FTL1バイオマーカー開発研究 – 参加条件:50歳以上の健康な成人
- 京都大学医学部附属病院 – 軽度認知障害患者を対象とした治験準備 – 2026年開始予定
- 東京大学医学部附属病院 – FTL1レベル測定システムの臨床評価 – 登録受付中
結論:人類の未来を変える科学の力
FTL1発見の歴史的意義
UCSF研究チームによるFTL1タンパク質の発見は、単なる科学的知見の蓄積を超えた、 人類の老化に対する根本的な理解の転換点となりました。
これまで「避けられない生物学的運命」と考えられてきた脳の老化が、実際には 制御可能で、逆転可能なプロセスであることが科学的に証明されました。この発見は、21世紀最大の医学的ブレークスルーの一つとして歴史に刻まれるでしょう。
実現される未来像
- 認知症のない社会 – アルツハイマー病の根本的治療と予防 – 高齢者の尊厳ある生活の実現
- 100歳時代の知的生産性 – 生涯を通じた学習と創造活動 – 経験と知識の社会への継続的貢献
- 世代を超えた家族の絆 – 認知機能を保った高齢者との深い交流 – 家族介護負担からの解放
私たちにできること
この革命的発見の恩恵を最大化するために、私たち一人ひとりができることがあります:
- 科学的情報への関心 – 研究の進展を継続的にフォロー – 信頼できる情報源からの学習
- 健康的ライフスタイルの実践 – FTL1抑制に効果的な生活習慣の採用 – 予防医学的アプローチの重視
- 研究支援への参加 – 臨床試験への協力検討 – 科学研究への理解と支援
FTL1タンパク質の発見は、私たちが「老化」という概念そのものを再定義し、 真に健康で充実した超長寿社会を実現するための扉を開きました。この科学の奇跡が、一人でも多くの人々の人生を豊かにし、人類全体の未来を明るく照らすことを心から願っています。


コメント